Báo Tiền Phong đưa tin chiều 17/2, Cục Quản lý Dược đã cấp giấy phép lưu hành có điều kiện cho thuốc điều trị COVID-19 Molnupiravir 400mg do Công ty TNHH Liên doanh Stellapharm Việt Nam sản xuất; thuốc Molravir 400mg của Công ty CP dược phẩm Boston Việt Nam và Movinavir của Công ty CP dược phẩm Mekorpha.
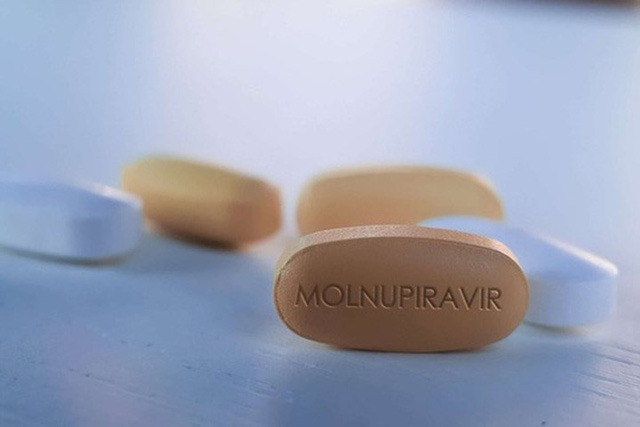
Đây là 3 đơn vị đủ điều kiện đã được Bộ Y tế cấp phép sản xuất thuốc Molnupiravir tại Việt Nam. Cục Quản lý Dược cũng yêu cầu 3 công ty sản xuất thuốc trong nước phối hợp với các cơ sở điều trị thực hiện đúng các quy định hiện hành về thuốc kê đơn, theo dõi an toàn, hiệu quả, tác dụng không mong muốn của thuốc kháng virus trên người Việt Nam và tổng hợp, báo cáo theo quy định tại Điều 5 Thông tư số 32/2018/TT-BYT.
Các đơn vị sản xuất phải kê khai giá thuốc và được thẩm định giá bởi cơ quan quản lý. Giá bán dự kiến thấp hơn nhiều so với nhập khẩu.
Theo Bộ Y tế, hiện nay, thuốc Molnupiravir đang được sử dụng trong Chương trình thí điểm điều trị có kiểm soát cho các trường hợp mắc COVID-19 thể nhẹ do Bộ Y tế triển khai, không bán trên thị trường.
Để đảm bảo an toàn cho người sử dụng và xử lý nghiêm các vi phạm trong việc kinh doanh thuốc, trước đó Cục Quản lý Dược đã có văn bản đề nghị Sở Y tế các tỉnh, thành phố tăng cường thanh tra, kiểm tra, xử lý nghiêm các vi phạm trong sản xuất, kinh doanh, thông tin quảng cáo thuốc dùng trong phòng, chống Covid-19 và xử lý nghiêm các vi phạm, đặc biệt các trường hợp kinh doanh thuốc không rõ nguồn gốc, tăng giá thuốc bất hợp lý.
Trường hợp phát hiện các hành vi vi phạm có dấu hiệu hình sự thì kịp thời chuyển cơ quan có thẩm quyền xử lý theo quy định.
Theo báo Người Lao Động, Bộ Y tế cũng cho biết thuốc kháng virus Molnupiravir được sử dụng để điều trị COVID-19 mức độ nhẹ đến trung bình ở người trưởng thành dương tính với xét nghiệm chẩn đoán SARS-CoV-2 và có ít nhất 1 yếu tố nguy cơ làm bệnh tiến triển nặng.
Molnupiravir dùng trên bệnh nhân có thời gian khởi phát triệu chứng dưới 5 ngày, không được sử dụng quá 5 ngày liên tiếp; không được sử dụng để dự phòng sau hay trước phơi nhiễm để phòng COVID-19.
Trước khi được cấp phép, Molnupiravir được thử nghiệm lâm sàng song song ở các nước Mỹ, Ấn Độ và thử nghiệm lâm sàng tại cơ sở thu dung điều trị của Bệnh viện Thống Nhất, Khoa Y tế công cộng Bệnh viện Đại học Y Dược TPHCM. Chương trình thử nghiệm đã được tiến hành với số lượng trên 80.000 bệnh nhân tại 51 tỉnh, thành phố trên cả nước.
Kết quả được Bộ Y tế công bố khi điều trị F0 trong cộng đồng, cho thấy Molnupiravir có tính an toàn cao, dung nạp tốt, hiệu quả rõ rệt về giảm tải lượng virus, giảm lây lan, giảm chuyển nặng, rút ngắn thời gian điều trị với tỷ lệ bệnh nhân có kết quả xét nghiệm RT-PCR sau 5 ngày âm tính; tỷ lệ chuyển nặng rất thấp từ 0,02%-0,06% và không có ca nào dẫn đến tử vong.
Molnupiravir 400 mg do Stellapharm sản xuất đã được đánh giá thực tế với công nhận kết quả thử nghiệm lâm sàng của Hội đồng Đạo đức Y sinh học Quốc gia cũng như giấy chứng nhận của Cục Khoa học Công nghệ và Đào tạo, Bộ Y tế.
Mộc Miên (T/h)